Του Θεόδωρου Δημούδη,
Ένα μεγάλο ποσοστό ανθρώπων γνωρίζει πως ο καρκίνος είναι μια ασθένεια που προκαλείται από μεταλλάξεις στο γενετικό υλικό του πυρήνα των κυττάρων, οι οποίες οδηγούν σε ανεξέλεγκτο κυτταρικό πολλαπλασιασμό και τη δημιουργία όγκου. Πολλά έχουν ειπωθεί για μεταλλάξεις σε υπεύθυνα γονίδια και άπλετο φως έχει ριχθεί στη γενετική συνιστώσα της νόσου. Ωστόσο, λίγοι έχουν ακούσει για μια διαφορετική προσέγγιση στον επιστημονικό κόσμο, που χαρακτηρίζει τον καρκίνο ως «μεταβολική νόσο», δηλαδή διαταραχή με κύριο γνώρισμα ανωμαλίες στις βιοχημικές αντιδράσεις του μεταβολισμού των κυττάρων.
Μεταβολισμός καρκινικών κυττάρων και φαινόμενο Warburg
Πράγματι, τα καρκινικά κύτταρα χρησιμοποιούν τα μακροθρεπτικά συστατικά που προσλαμβάνονται από τη διατροφή με τρόπο διαφορετικό από τα υγιή κύτταρα, με στόχο να παράγουν την ενέργεια που χρειάζονται για τη λειτουργία τους. Για να γίνει αυτό κατανοητό, θα αναφερθούμε στη γλυκόζη. Η γλυκόζη είναι το κύριο καύσιμο μόριο του οργανισμού και ο σημαντικότερος υδατάνθρακας, αφού τα κύτταρα την αξιοποιούν ως την πρωταρχική πηγή ενέργειας μέσω της διαδικασίας αποικοδόμησής της, τη γλυκόλυση. Όμως, η κατάληξη του προϊόντος της γλυκόλυσης, δηλαδή του πυροσταφυλικού, εξαρτάται από τη διαθεσιμότητα του οξυγόνου. Έτσι, παρουσία οξυγόνου το πυροσταφυλικό θα μεταβολιστεί περαιτέρω σε άλλες βιοχημικές πορείες για επιπρόσθετη παραγωγή ενέργειας, ενώ απουσία οξυγόνου θα καταλήξει μέσω ζυμώσεων σε αιθανόλη ή γαλακτικό οξύ. Το παράδοξο είναι πως τα ταχέως αυξανόμενα καρκινικά κύτταρα θα μεταβολίσουν τη γλυκόζη σε γαλακτικό ακόμα και παρουσία οξυγόνου, μια πορεία που ονομάζεται «φαινόμενο Warburg», από τον βιοχημικό Dr. Otto Warburg (βραβείο Νόμπελ 1931).
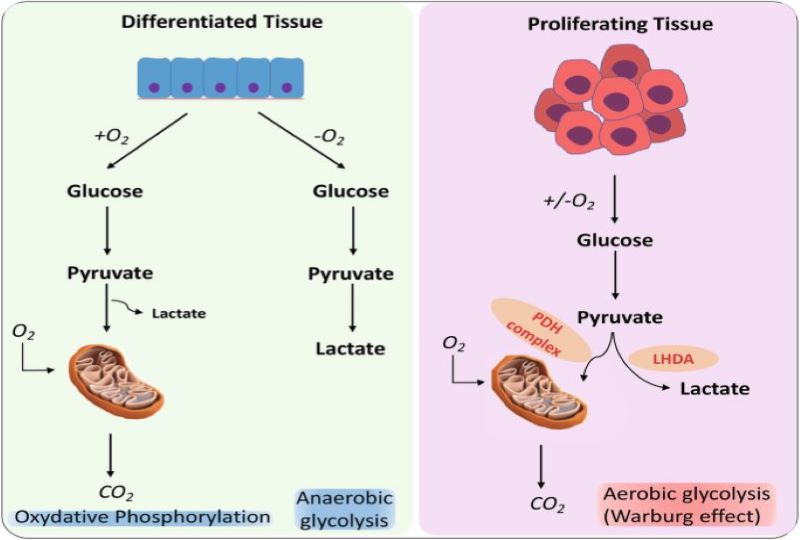
Τα πλεονεκτήματα που προσφέρει στον όγκο αυτή η προσαρμογή συνοψίζονται παρακάτω:
- Το γαλακτικό οξύ που παράγεται μετατρέπει το περιβάλλον του όγκου σε όξινο, γεγονός που διευκολύνει τη διήθησή του κάνοντάς τον πιο μεταστατικό. Επίσης, εξασθενίζει την ενεργοποίηση των CD8+ T και των ΝΚ κυττάρων του ανοσοποιητικού συστήματος.
- Η αυξημένη πρόσληψη γλυκόζης προμηθεύει υποστρώματα για τη μεταβολική πορεία των φωσφορικών πεντοζών, η οποία δημιουργεί βιοσυνθετική ενέργεια (μέσω NADPH) για τη σύνθεση λιπιδίων και αμινοξέων που θα χρειαστούν τα νέα καρκινικά κύτταρα.
- Τα καρκινικά κύτταρα αυξάνονται ταχύτερα από τα αιμοφόρα αγγεία που τα προμηθεύουν με οξυγόνο, με αποτέλεσμα να εμφανίζουν υποξία. Συνεπώς, η ελαττωμένη εξάρτηση της κυτταρικής αύξησης από το οξυγόνο είναι απαραίτητη για την επιβίωσή τους.
Ο ρόλος των μιτοχονδρίων
Τα μιτοχόνδρια είναι οργανίδια του κυττάρου με βασικό ρόλο την παραγωγή ενέργειας από την οξείδωση των τροφίμων, μέσω των βιοχημικών μονοπατιών του κύκλου του Krebs και της οξειδωτικής φωσφορυλίωσης. Διαταραχές στα ενδιάμεσα στάδια του κύκλου του Krebs συνδέονται άμεσα με την καρκινογένεση. Για παράδειγμα, όταν συσσωρεύονται ενδιάμεσοι μεταβολίτες, λόγω δυσλειτουργίας κάποιου ενζύμου του κύκλου, διαχέονται στο εσωτερικό του κυττάρου και δημιουργούν ένα περιβάλλον ψευδο-υποξίας που επιφέρει τη μετατροπή του κυττάρου σε καρκινικό. Υπό αυτές τις συνθήκες, τα κύτταρα παράγουν μικρό ποσό ενέργειας από τον μεταβολισμό της γλυκόζης και οδηγούνται στην κατανάλωση τεράστιων ποσοτήτων αυτής για να καλύψουν τις ανάγκες τους. Το συγκεκριμένο χαρακτηριστικό των καρκινικών κυττάρων χρησιμοποιείται και στην εξέταση PET scan, όπου χορηγείται ραδιενεργά σεσημασμένη γλυκόζη και, στη συνέχεια, εντοπίζονται τα σημεία αυξημένης συγκέντρωσης της γλυκόζης, που αντιστοιχούν σε καρκινικά κύτταρα.
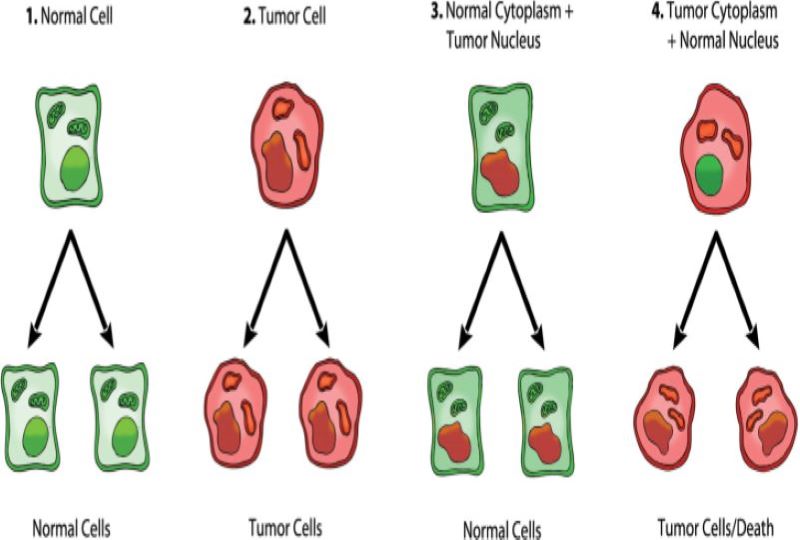
Για μια μερίδα επιστημόνων, ο πρωταρχικός παράγοντας στην ανάπτυξη του καρκίνου είναι η μιτοχονδριακή δυσλειτουργία, η οποία μπορεί να προκληθεί από διάφορους παράγοντες (ακτινοβολία, χημικές ουσίες, μεταλλάξεις). Πιο συγκεκριμένα, τα δυσλειτουργικά μιτοχόνδρια παράγουν ενώσεις που ονομάζονται δραστικές μορφές οξυγόνου (ROS) που μπορούν να βλάψουν το DNA μας και να δημιουργήσουν δευτερεύουσες γενετικές μεταλλάξεις, που θα έχουν ως επακόλουθο την ογκογένεση. Η υπόθεση της πρωταρχικής σημασίας των μιτοχονδρίων στον καρκίνο αποδεικνύεται και πειραματικά, αφού μελέτες έδειξαν πως εάν ο πυρήνας που περιέχει γενετικές μεταλλάξεις για καρκινική ανάπτυξη μεταφερθεί σε φυσιολογικό κυτταρόπλασμα (περιέχει τα μιτοχόνδρια), τότε θα παραχθούν μόνο φυσιολογικά κύτταρα. Αντιθέτως, η μεταφορά ενός πυρήνα φυσιολογικού κυττάρου σε ένα κυτταρόπλασμα κυττάρων όγκου γεννά κύτταρα όγκου ή νεκρά κύτταρα, αλλά όχι φυσιολογικά. Επομένως, υποδηλώνεται ότι οι γενετικές μεταλλάξεις στο πυρηνικό DNA δεν αρκούν για τη δημιουργία νεοπλασιών, καθώς και ότι τα φυσιολογικά μιτοχόνδρια μπορούν να καταστείλουν την ογκογένεση.
Η σημασία της διατροφής
Η μεταβολική θεωρία ανάπτυξης του καρκίνου έχει δημιουργήσει πρόσφορο έδαφος για την επινόηση διατροφικών προσεγγίσεων με σκοπό τον περιορισμό και την αντιμετώπιση της νόσου. Καθώς η γλυκόζη είναι το κύριο καύσιμο για τον μεταβολισμό της ενέργειας του όγκου μέσω της γαλακτικής ζύμωσης, ο περιορισμός της γλυκόζης γίνεται πρωταρχικός στόχος. Ωστόσο, τα περισσότερα φυσιολογικά κύτταρα του σώματος χρειάζονται, επίσης, προϊόντα γλυκολυτικής οδού, όπως το πυροσταφυλικό, για την παραγωγή ενέργειας μέσω της οξειδωτικής φωσφορυλίωσης. Το πρόβλημα αυτό λύνει η κετογονική διατροφή χαμηλής περιεκτικότητας σε υδατάνθρακες και ζάχαρη και υψηλής σε λιπαρά. Όταν η διαθεσιμότητα της γλυκόζης περιοριστεί, τα περισσότερα φυσιολογικά κύτταρα θα αρχίζουν να μεταβολίζουν λίπη και κετονοσώματα. Τα κετονοσώματα παράγονται στο ήπαρ από τριακυλογλυκερόλες κατά τη διάρκεια περιόδων νηστείας. Ο περιορισμός της συνολικής θερμιδικής πρόσληψης θα διευκολύνει τη μείωση των επιπέδων γλυκόζης και ινσουλίνης στο αίμα και αύξηση των κετονοσωμάτων (β-υδροξυβουτυρικό και ακετοξικό). Τα περισσότερα καρκινικά κύτταρα δε μπορούν να χρησιμοποιήσουν κετονοσώματα για ενέργεια λόγω ανωμαλιών στη δομή ή τη λειτουργία των μιτοχονδρίων και έτσι, θα οδηγηθούν σε θάνατο. Ως εκ τούτου, το μεταβολικό στρες θα είναι μεγαλύτερο στα καρκινικά παρά στα φυσιολογικά κύτταρα, όταν ολόκληρο το σώμα απομακρύνεται από τη γλυκόζη στα κετονοσώματα για ενέργεια.
Ενθαρρυντικές είναι και οι ενδείξεις της διαλειμματικής νηστείας. Η στέρηση τροφής για μικρά διαστήματα οδηγεί τον οργανισμό σε αερόβιες διαδικασίες που συμφέρουν ενεργειακά. Τέτοια διαιτητικά σχήματα προκαλούν ευρείες αλλαγές στους αυξητικούς παράγοντες και στα επίπεδα μεταβολιτών, μειώνοντας, έτσι, την ικανότητα των καρκινικών κυττάρων να επιβιώνουν από τις χημειοθεραπείες. Οι νηστείες ή οι δίαιτες που μιμούνται τις νηστείες αυξάνουν επιπλέον την αντίσταση των φυσιολογικών κυττάρων στη χημειοθεραπεία, αλλά όχι και των καρκινικών, προάγοντας την αναγέννηση φυσιολογικών ιστών, γεγονός που θα μπορούσε να βοηθήσει στην πρόληψη και αποφυγή επιβλαβών και δυνητικά απειλητικών για τη ζωή παρενεργειών που προκαλούν οι θεραπείες. Σε μια μελέτη, ασθενείς που διαγνώστηκαν με μια ποικιλία κακοηθειών υποβλήθηκαν εθελοντικά σε νηστεία πριν από (48-140 ώρες) ή/και μετά από χημειοθεραπεία (5-56 ώρες). Κανένας από αυτούς τους ασθενείς, που έλαβαν κατά μέσο όρο 4 σχήματα διαφόρων φαρμάκων χημειοθεραπείας σε συνδυασμό με νηστεία, δεν ανέφερε σημαντικές παρενέργειες εκτός από την πείνα και τη ζαλάδα.

Συνοψίζοντας, οι ανθρώπινοι καρκίνοι εξελίσσονται σε ένα περιβάλλον μεταβολικού στρες. Ταχέως πολλαπλασιαζόμενα καρκινικά κύτταρα τα οποία στερούνται επαρκούς οξυγόνου, θρεπτικών ουσιών, ορμονών και αυξητικών παραγόντων, ρυθμίζουν ανοδικά τα βιοχημικά μονοπάτια που καλύπτουν αυτές τις ανεπάρκειες για να ξεπεράσουν την υποξία. Η επιδιόρθωση αυτών των μεταβολικών διαταραχών με διαιτητικά πρωτόκολλα που θα επιδρούν σε συνδυασμό με γνωστά θεραπευτικά σχήματα, φαίνεται να είναι ένα πολλά υποσχόμενο πεδίο έρευνας. Ενδεχομένως με αυτή την αντιμετώπιση, να φτάσουμε ένα βήμα πιο κοντά στην εξάλειψη της επάρατης αυτής νόσου.
ΕΝΔΕΙΚΤΙΚΕΣ ΠΗΓΕΣ
- Seyfried TN, Flores RE, Poff AM, D’Agostino DP. Cancer as a metabolic disease: implications for novel therapeutics, 2014. Διαθέσιμο εδώ
- Nencioni, A., Caffa, I., Cortellino, S. et al.Fasting and cancer: molecular mechanisms and clinical application. Nat Rev Cancer 18, 707–719 (2018). Διαθέσιμο εδώ
- ΚΑΡΚΙΝΟΣ ΚΑΙ ΜΙΤΟΧΟΝΔΡΙΑ, metabolomicmedicine.com. Διαθέσιμο εδώ
- Η άποψη ογκολόγων ερευνητών σε ότι αφορά την αιτία ανάπτυξης του καρκίνου και το ρόλο της διατροφής, karagiannisathanasios.gr. Διαθέσιμο εδώ
- Η «διαλλειμματική» νηστεία «στραγγαλίζει» τα καρκινικά κύτταρα, in.gr. Διαθέσιμο εδώ
- Berg, J., Tymoczko, J., Gatto, G.J., Stryer, L., Βιοχημεία, Πανεπιστημιακές Εκδόσεις Κρήτης, 2021